لماذا يمكن أن يعود السرطان بعد سنوات

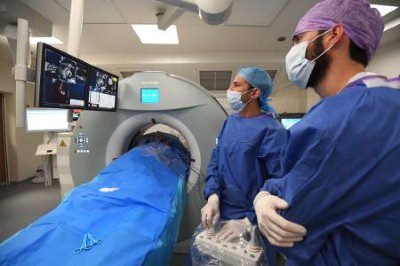
Cancer cells can reawaken after a period of dormancy, triggering a relapse. Credit: Science History Images/Alamy
عندما تم إعلان خلو ليزا داتون من سرطان الثدي وفي عام 2017، خصصت بعض الوقت للاحتفال مع العائلة والأصدقاء، على الرغم من أنها علمت أن رحلتها مع السرطان قد لا تنتهي. يرى ما يصل إلى ثلث الأشخاص الذين تم شفاء أورام ثديهم يعود المرضوأحياناً بعد عقود من الزمن. ومن المعروف أن العديد من أنواع السرطان الأخرى تتكرر في السنوات التالية للعلاج الأولي، وبعضها بمعدلات أعلى بكثير.
يقول داتون، مستشار إدارة الرعاية الصحية المتقاعد الذي يعيش في فيلادلفيا، بنسلفانيا: «إن الأمر دائمًا ما يكون في الجزء الخلفي من عقلك، وقد يكون ذلك مرهقًا».
يمكن قريبًا هندسة الخلايا المناعية المقاومة للسرطان داخل أجسامنا
وكجزء من علاجها، التحقت داتون بتجربة سريرية تسمى SURMOUNT. وهذا من شأنه أن يراقبها بحثًا عن الخلايا السرطانية النائمة، والتي يعتقد العديد من الباحثين الآن أنها قد تفسر على الأقل بعض تكرار الإصابة بالسرطان1. تتهرب هذه الخلايا السرطانية النائمة من العلاج الأولي وتنتقل إلى أجزاء أخرى من الجسم. بدلًا من التكاثر لتكوين الأورام على الفور، كما هو معتاد سرطان النقيليحيث تنتشر الخلايا من الورم الرئيسي — وتبقى الخلايا النائمة نائمة. يخفون من الجهاز المناعي وليس تقسيم بنشاط. ولكن في وقت لاحق، يمكن أن تستيقظ من جديد وتؤدي إلى ظهور الأورام.
على الرغم من أن داتون أدركت أن علاجها ربما لم يزيل جميع علامات السرطان، إلا أنها تقول إنها أصيبت بالصدمة في عام 2020 عندما تم العثور على خلايا نائمة في نخاع عظامها لأول مرة.
يكتشف الباحثون خلايا سرطانية نائمة، تُعرف أيضًا باسم الخلايا السرطانية المنتشرة، مرتبطة بالثدي والبروستاتا والرئة والقولون.2 وغيرها من أنواع السرطان، وهذه الخلايا متورطة بشكل متزايد في بعض أنواع السرطان النقيلي. ما يقدر بنحو 30% من الأشخاص الذين تم علاجهم بنجاح من السرطان قد يكون لديهم هذه الخلايا، على الرغم من أن الأبحاث غير المنشورة تشير إلى أنها قد تكون أكثر شيوعًا.
على مدى العقد الماضي، حاولت سلسلة من الجهود التعرف على الخلايا النائمة وفهمها، بهدف نهائي هو معالجتها. وتجري الآن مجموعة من التجارب السريرية لاختبار العلاجات المحتملة.
على الرغم من أن التجربة الأولى التي اشتركت فيها داتون كانت تراقب الخلايا فقط، فقد سجلت منذ ذلك الحين تجربة ثانية تسمى CLEVER تهدف إلى القضاء على الخلايا.3. ومع المضي قدمًا في مثل هذه التجارب، فإن الأسئلة المفتوحة حول الخلايا النائمة، بما في ذلك ما الذي يسبب السكون وكيفية محاربته، تجذب المزيد من الباحثين إلى هذا المجال.
يقول سايروس غاجار، عالِم بيولوجيا السرطان في مركز فريد هاتشينسون للسرطان في سياتل بواشنطن: «لقد بدأنا نرى مجموعات متعددة تتقارب حول بعض الأفكار نفسها، وهو ما يكون دائمًا مؤكدًا للغاية». إن المحاكمات الجارية هي “شهادة على مدى التقدم الذي تم إحرازه”.
تهديد صامت
تم اقتراح وجود خلايا سرطانية نائمة في وقت مبكر من ثلاثينيات القرن العشرين، عندما عزا عالم الأمراض الأسترالي روبرت ويليس بعض حالات النمو السرطاني الثانوي إلى مثل هذه الخلايا.4. ومع بدء حياة الأشخاص الذين عولجوا من السرطان لفترة أطول، لاحظ هو وآخرون أن المرض يعود أحيانًا في وقت لاحق بكثير، وغالبًا ما يكون أكثر عدوانية. وعلى الرغم من هذا الاقتراح المبكر، فإن فكرة السكون لم تنتشر لعقود من الزمن.
يتذكر لويس تشودوش، وهو طبيب وعالم بجامعة بنسلفانيا في فيلادلفيا، أنه واجه مقاومة عندما بدأ مناقشة الفكرة مع زملائه منذ أكثر من 20 عامًا. ويقول إنه لا أحد يريد أن يصدق أن الأدوية التي تقتل السرطان قد تترك شيئًا ما وراءها، ولم تكن شركات الأدوية مهتمة بتطوير علاجات للأشخاص الذين يبدو أنهم قد تم شفاؤهم. وقال العديد من العلماء في ذلك الوقت إن السرطانات المتكررة يجب أن تكون جديدة، وليست مرتبطة بأي تشخيصات سابقة.
يقول تشودوش، وهو باحث مشارك في دراسات SURMOUNT وCLEVER، جنبًا إلى جنب مع أنجيلا ديميشيل، طبيبة الأورام في كلية بيرلمان للطب بجامعة بنسلفانيا: “فقط عندما تتراكم أدلة كافية، يتم دفعك بعيدًا عن طريقة التفكير هذه”.
تبحث أنجيلا ديميشيل (يسار) ولويس تشودوش عن طرق لاستهداف الخلايا السرطانية النائمة.الائتمان: بيجي بيترسون لبن ميدسين
وباستخدام عدد قليل من العلامات الخلوية، تمكن الباحثون الآن من تحديد الخلايا السرطانية النائمة في أجزاء كثيرة من الجسم5. يمكن لهذه العلامات أن تخبر العلماء ليس فقط ما إذا كانت الخلايا تنمو وتنقسم، ولكن أيضًا أين نشأت الخلايا وبالتالي أي نوع من السرطان إنهم مرتبطون بـ. ومع ذلك، فإن الأساليب ليست مثالية، ولا يزال الباحثون يحاولون تحديد ما إذا كانت خلايا معينة أكثر عرضة للدخول في حالة سبات أكثر من غيرها، وما هي الميزات التي تحدد هذه الخلايا.
وقد وجد غجر وآخرون أن الخلايا النائمة تترك الورم الرئيسي في وقت مبكر من تطور السرطان، وغالبًا قبل تشخيص المرض.6. ليس من الواضح تمامًا كيف ولماذا تنفصل هذه الخلايا، ولكن بعد قضاء دقائق فقط في الدورة الدموية، تخرج من مجرى الدم وتتركز في أجزاء معينة من الجسم، مثل نخاع العظم والغدد الليمفاوية. ويقول إنه حتى في هذه البيئات، تكون الخلايا الخاملة نادرة للغاية، حيث لا تتجاوز حفنة من بين ملايين الخلايا السليمة. إن حالة توقف الحركة لديهم تحميهم من العلاجات التقليدية، مثل العلاج الكيميائي، الذي يستهدف الخلايا سريعة الانقسام.
يقول بيتروس تسانتوليس، طبيب الأورام بجامعة جنيف في سويسرا، إن فترة السكون تختلف عن فترة السكون. حالات أخرى معروفة مثل الشيخوخةحيث تتوقف الخلايا القديمة عن الانقسام بينما تستعد للموت. وفي ظل الظروف المناسبة، يمكن للخلايا النائمة أن تبدأ بالانقسام من جديد. وبمجرد استيقاظها من جديد، تتكاثر الخلايا النائمة لتشكل أورامًا تكرر التعقيد الكامل للورم الأصلي.
وقد دفع هذا بعض الباحثين إلى اقتراح أن الخلايا السرطانية النائمة قد تكون خلايا جذعية سرطانية، وهي نوع من الخلايا التي من خلال التجديد والتمايز قد تؤدي إلى ظهور الورم – أو أنها، على الأقل، قد تكون خلايا سرطانية ذات سمات تشبه الجذع.
ننسى سرطان الرئة أو الثدي أو البروستاتا: لماذا يجب تغيير تسمية الورم
تتميز الخلايا السرطانية النائمة ببعض الخصائص التي ترتبط عادةً بالخلايا الجذعية، مثل الإفراط في التعبير عن جينات معينة. يقول عالم الأحياء السرطاني جوان ماساجو، مدير معهد سلون كيترينج في مدينة نيويورك، إن الخلايا الجذعية تقضي معظم وقتها في حالة سبات، ولا تستيقظ إلا بعد الإصابة أو المرض، مما يجعلها مرشحة واضحة. ومع ذلك، فإن وجود الخلايا الجذعية السرطانية ما زال فكرة مثيرة للجدل.
يبدو أن العلماء مستعدون لحل بعض هذه الأسئلة المفتوحة قريبًا. بتقنيات مخبرية متقدمة تمنح الباحثين القدرة على ذلك دراسة الخلايا الفردية وبشكل أوثق، أصبح من الممكن الآن تحديد الخلايا السرطانية النائمة وعزلها وإثرائها لمزيد من الدراسة. على سبيل المثال، يقوم فريق تشودوش وديميكيلي بتطوير اختبار لتحديد الخلايا النائمة. يقول تشودوش إنها أكثر حساسية بكثير من الأساليب الحالية، وقد تؤدي في نهاية المطاف إلى تحسين تقديرات عدد الأشخاص الذين يؤويون خلايا نائمة.
في هذه الأثناء، استقر غجر على طريقة مختلفة للتفكير بشأن هذه الخلايا. على سبيل المثال، إذا وصلت خلية خاملة من ورم في الثدي إلى نخاع العظم، فمن المتوقع أن تحتفظ بالعديد من سمات خلية سرطان الثدي التي من شأنها أن تمكن من التعرف عليها. يقول غجر: “لكن ما نكتشفه هو أن هذه التوقعات لا تصمد”، مشيرًا إلى أنه بمجرد انتشار الخلية السرطانية، فإنها غالبًا ما تغير شكلها وحجمها وسلوكها. “سيتعين علينا أن نذهب إلى ما هو أبعد من التعريف القائم على السمات الموحدة، وبدلاً من ذلك نرسم خريطة للطفرات في هذه الخلايا إلى طفرات في الورم الأصلي – لتحديد الخلية المنتشرة ليس بالشكل الذي نعتقد أنه يجب أن تبدو عليه، ولكن بما يخبرنا به جينومها.”
إشارات النوم والاستيقاظ
وبعيدًا عن تعريف السكون، يريد الباحثون أن يفهموا كيف ولماذا تدخل الخلايا في حالة سبات، وما هي أنواع المحفزات التي توقظها من جديد.
وفقًا لجوديث أجودو، عالمة المناعة في معهد دانا فاربر للسرطان في بوسطن، ماساتشوستس، من المحتمل أن تدخل الخلايا في حالة سبات كإجراء وقائي. وتقول إن الخلايا الفردية، كجزء من الورم، قد تكون معزولة عن هجوم الجهاز المناعي، ولكن بمجرد أن تصبح مستقلة، “يمكن التقاطها بسهولة دون اتخاذ خطوات لإخفاء نفسها”. بالإضافة إلى ذلك، فإن الرحلة عبر الجسم إلى مكان جديد هي رحلة مرهقة تقتل الغالبية العظمى من الخلايا التي تنفصل. السكون هو إحدى طرق الاستمرار في بيئة قاسية.
أظهرت الأبحاث أنه بينما تكون الخلايا نائمة، فإنها تستمر في الانخراط في الحديث المتبادل مع بيئتها الدقيقة7 وتعديل أنفسهم للحفاظ على السكون بشكل فعال. على سبيل المثال، يبدو أن الخلايا النائمة تغير أنماط التعبير للجينات المشاركة في بقاء الخلية، بما في ذلك المنظم المركزي لاستقلاب الخلية ونموها الذي يسمى مسار mTOR8. تستغل الخلايا أيضًا شكلاً من أشكال إعادة التدوير الذاتي يسمى الالتهام الذاتي – حرفيًا “الأكل الذاتي” – والذي يسمح للخلايا النائمة بإعادة استخدام الموارد الداخلية والبقاء على قيد الحياة مع القليل من المدخلات من البيئة المحيطة بها.9.
يبدو أن الخلايا لديها علاقة معقدة مع بيئتها الخارجية أيضًا، بما في ذلك جهاز المناعة. يقول خوليو أغيري غيسو، المدير المؤسس لمعهد سكون السرطان في مركز مونتيفيوري أينشتاين الشامل للسرطان في مدينة نيويورك، إن الاستجابة المناعية متورطة ليس فقط في إحداث السكون، ولكن أيضًا في الحفاظ عليه وإنهائه.
لقد أظهر هو وفريقه أن الخلايا البلعمية في الرئتين تنتج بروتينًا معينًا يرتبط بخلايا سرطان الثدي النائمة ويعزز السكون10. وقد أظهرت أبحاث أخرى كيف يمكن للخلايا النائمة أن تتهرب من مراقبة خلايا الجهاز المناعي، بما في ذلك الخلايا التائية11 والخلايا القاتلة الطبيعية12.
تشير الأبحاث مجتمعة إلى أن الخلايا غالبًا ما تظل خاملة حتى يتم تعطيل المشهد المناعي بطريقة ما، مما يؤدي إلى تغيير التوازن بما يكفي لإيقاظ الخلايا بأمان. قد تنطوي هذه التحولات على الإصابة أو المرض، حيث ربطت الدراسات التي أجريت في السنوات القليلة الماضية بين تلف الخلايا13 وكوفيد-19 وعدوى الأنفلونزا14 للهروب من السكون . الشيخوخة والتليف15, الإجهاد المزمن أو قد تساهم خيارات نمط الحياة أيضًا في الاستيقاظ.
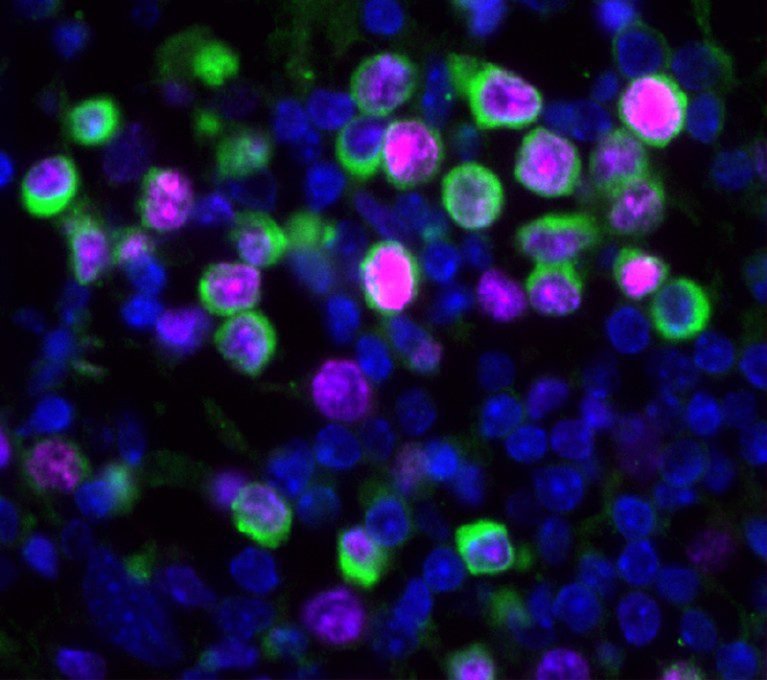
يمكن لعدوى الأنفلونزا أن تجبر الخلايا السرطانية النائمة على البدء في النمو والانقسام (الأخضر).الائتمان: بريان جونسون
تقول شيلي بايتون، مهندسة الطب الحيوي بجامعة تافتس في ميدفورد، ماساتشوستس، إنه بالنسبة للخلايا «إنها لعبة احتمالات». تحاول الخلايا باستمرار الخروج من حالة السكون بعد حدوث اضطرابات صغيرة، ليتم قتلها. وتقول: “لكن في اللحظات التي يختل فيها التوازن، غالبًا ما نرى انتشار النقائل”.
يركز عمل بيتون على التليف، وهو تراكم النسيج الضام الليفي في الموقع التالف. وغالبًا ما يرتبط هذا بالسرطان، لأن التيبس يساعد الورم على النمو ويساعد في إرسال الإشارات بين الخلايا. لكن النخاع العظمي، حيث تتواجد الخلايا النائمة في كثير من الأحيان، يكون طريًا، ويهتم بيتون بما إذا كانت تلك البيئة الناعمة قد تكون إحدى السمات التي تعزز السكون. وتقول إنه من الممكن أن يؤدي فقدان كثافة العظام الطبيعية المرتبطة بالعمر (هشاشة العظام) أو التغيرات الهرمونية لدى النساء اللاتي أصبن سابقًا بسرطان الثدي إلى التليف، وربما إيقاظ السرطان من جديد.
■ مصدر الخبر الأصلي
نشر لأول مرة على: www.nature.com
تاريخ النشر: 2026-01-06 02:00:00
الكاتب: Amanda Heidt
تنويه من موقع “yalebnan.org”:
تم جلب هذا المحتوى بشكل آلي من المصدر:
www.nature.com
بتاريخ: 2026-01-06 02:00:00.
الآراء والمعلومات الواردة في هذا المقال لا تعبر بالضرورة عن رأي موقع “yalebnan.org”، والمسؤولية الكاملة تقع على عاتق المصدر الأصلي.
ملاحظة: قد يتم استخدام الترجمة الآلية في بعض الأحيان لتوفير هذا المحتوى.